segunda-feira, 11 de março de 2013
ATPS (II e III Períodos)
Para as informações completas de seu ATPS, por favor, acesse os links
As discussões sobre cada ATPS procederão nesta semana.
QUÍMICA ORGÂNICA 1
https://docs.google.com/file/d/0B_37aA1dYynoSURfelhDOFRHZms/edit?usp=sharing
Se você tiver problemas para abrir os arquivos pelo link dos pdfs, acesse esses aqui:
Passo 1 (Aluno)
Ler o texto “Introdução à Química Orgânica”. Disponível em:
<http://docs.google.com/fileview?id=0B6JWjCyayLXMNTE0ZWJmNGItMTg5Mi00YmVjLTkwN2EtYTMwMjk3YWEyZTZj&hl=pt_PT>. Acesso em: 23 mar. 2012.
Passo 2 (Aluno)
<https://docs.google.com/file/d/0B6JWjCyayLXMZVZxSkUxN0pTMGlxS29CbzlrZU8yZw/edit>
Passo 3 (Aluno)
Assistir o vídeo “O átomo de carbono”. Disponível em:
<https://docs.google.com/file/d/0B6JWjCyayLXMYUlKS2hPa1VUaWFMdkpRaHFXeEFM
dw/edit>. Acesso em: 23 mar. 2012.
BIOESTATÍSTICA
https://docs.google.com/file/d/0B_37aA1dYynoY2lfQlV5S2VFSmM/edit?usp=sharing
A Estatística no cotidiano escolar, de Raul Cuore. Disponível em:
<https://docs.google.com/viewer?a=v&pid=explorer&chrome=true& srcid=0B0EMRzdACiXpODJlNjYwZmMtMzNhOS00NGY2LWEyZTctMjI5ODA3NjBiODc2&hl=pt_BR>.
Acesso em: 20 mar. 2012.
Conceito e aplicações da Estatística. Disponível em:
<https://docs.google.com/viewer?a=v&pid=explorer&chrome=true&srcid=0B0EMRzdACiXpYmZhN2VjN2ItNWU2OC00YjI1LTkzNzQtNzM3YjA0ZDhhOGMz&hl=pt_BR >.
Acesso em: 20 mar. 2012.
FÍSICO-QUÍMICA
https://docs.google.com/file/d/0B_37aA1dYynoUFc0MzQ3RmdJZlk/edit?usp=sharing
sábado, 23 de fevereiro de 2013
Eu jamais passarei para medicina
Eu jamais passarei para medicina!!!!
Hei!!! Lembrem-se: até o nosso primeiro passo após o engatinhar nos pareceu tão desafiante! E hoje esse ato é tão rotineiro que nem nos damos conta de sua complexidade. E as nossas primeiras letras, a primeira frase, quanto sofrimento! E hoje juntar as letras e perceber o significado das palavras é trivial. Então meus caros, lembrem-se: Não há nada tão fácil que não seja um desafio, nem tão difícil que seja intransponível! O que nos nutre é o que desejamos ser! E a nossa força é do tamanho de nossos desejos!
Um abraço e bons estudos.
Fabio Costa
Talvez essa frase tenha passado por sua cabeça e você simplesmente aceitou esse “fato”, - eu jamais passarei para medicina! Eu jamais passarei para ..., seja lá o que for, essa sentença é tão verdadeira quanto você a desejar torná-la real! A maioria das limitações está em nós e não naquilo que julgamos impossível.
Hei!!! Lembrem-se: até o nosso primeiro passo após o engatinhar nos pareceu tão desafiante! E hoje esse ato é tão rotineiro que nem nos damos conta de sua complexidade. E as nossas primeiras letras, a primeira frase, quanto sofrimento! E hoje juntar as letras e perceber o significado das palavras é trivial. Então meus caros, lembrem-se: Não há nada tão fácil que não seja um desafio, nem tão difícil que seja intransponível! O que nos nutre é o que desejamos ser! E a nossa força é do tamanho de nossos desejos!
E o tempo? Ele é algo que os Homens inventaram, então dizer um não tenho tempo é dizer a si mesmo: - eu não quero fazer!
Um abraço e bons estudos.
Fabio Costa
domingo, 17 de fevereiro de 2013
O que é caráter iônico?
O que é o caráter iônico? Isso está relacionado com a ligação covalente? Sim, e veremos por qual razão.
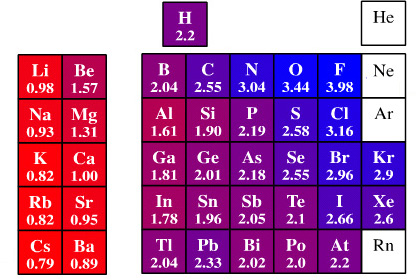
Em linhas gerais, o caráter iônico está relacionado a uma ligação química e é nesses termos que ele nos é útil. Os átomos se ligam graças a uma atração eletrostática entre eles. Essa ligação acontecerá se for energeticamente favorável ao sistema, isto é, se acarretar na diminuição da energia potencial eletrostática de seus elétrons de valência. Há três tipos de ligações (iônica, covalente e metálica). Embora em geral uma ligação tenha uma mistura de dois ou dos três tipos, essa classificação é aceita. Há casos que nosso interesse é inferir sobre o caráter covalente (compartilhar elétrons de valência) ou iônico (transferência de elétrons de valência) da ligação, ou seja se haverá um compartilhamento ou uma transferência de elétrons de valência. Assim precisamos de uma medida quantitativa para nos guiar. Para tanto usa-se a diferença de eletronegatividade dos átomos participantes de uma ligação, normalmente a escala de Pauling é a escolhida (resultados semelhantes são obtidos com a de Mulliken e de Allred-Rochow). Embora não exista qualquer linha divisória clara entre as ligações covalentes e iônicas, uma regra útil diz que, se a diferença de eletronegatividade é de cerca de 2 unidades, o caráter iônico é tão alto que é melhor considerar a iônica a ligação, como no NaCl e o KF (veja a tabela), por exemplo.
quinta-feira, 7 de fevereiro de 2013
Santa Maria 2013: Mais um tragédia anuncida
Cianeto de hidrogênio e a tragédia de Santa Maria
Uma lamentável sequencia de erros, descaso e despreparos ceifou a vida de centenas de jovens brasileiros, isso marcará para sempre a nossa memória. A dor que sentimos não se compara à dos que perderam os seus entes queridos. Lá se foram filhos e filhas que viveram o sonho da universidade pública de qualidade, e que muitas vezes também eram os dos pais. Nada será como antes não há remédio para essa dor. O que faremos em contrapartida? Estamos às portas de mais um carnaval, e é claro que temos direito ao nosso momento. Eu volto à pergunta, o que faremos? Pelo os que se foram, por eles deveras não há o que fazer, infelizmente. Mas não podemos fechar os olhos para o que nos cerca, a precariedade e insegurança de casas e estabelecimentos sem a menor condição de funcionamento é uma sentença de morta que paira sobre nossas cabeças. Vamos nos valer de nossos direitos, devemos exigir que essas casas cumpram a lei. Se deixarmos de frequentá-las ou elas fecharão ou se adequarão à lei.
Eu transcrevo um texto sobre os perigos do cianeto de hidrogênio, gás tóxico que supostamente foi o grande vilão dessa tragédia história. Presente na pirólise a 800ºC da espuma de poliuretano como resultando combustão de plásticos contendo grupos nitrila, o cianeto de hidrogênio (HCN) é letal dependendo do tempo de exposição.
Eu transcrevo um texto sobre os perigos do cianeto de hidrogênio, gás tóxico que supostamente foi o grande vilão dessa tragédia história. Presente na pirólise a 800ºC da espuma de poliuretano como resultando combustão de plásticos contendo grupos nitrila, o cianeto de hidrogênio (HCN) é letal dependendo do tempo de exposição.
Os sintomas de envenenamento por cianeto após a inalação dos
seus vapores surgem muito rapidamente e a sua severidade está diretamente
relacionada com a concentração do gás cianídrico no ambiente. Após várias horas
de exposição a concentrações atmosféricas menores que 50 ppm, os pacientes
desenvolvem sentimentos de ansiedade, inquietação, palpitações e dores de
cabeça. A sua recuperação pode no entanto ser rápida uma vez terminada a exposição,
contudo se esta exposição se prolongar, mesmo com doses baixas, pode ser fatal.
Uma exposição superior a 30 minutos a uma concentração
atmosférica de 100 ppm pode conduzir à morte. Doses mais elevadas que esta
levam ao rápido surgimento de taquicardia, dispneia, síncope (morte aparente ou
real, súbita por paralisia cardíaca) e tonturas. Estes sinais de envenenamento
podem também desaparecer rapidamente uma vez terminada a exposição. Em casos
mais graves a taquicardia é seguida de bradicardia que pode progredir para um
estado de dissistolia (astenia
cardiovascular). Quando as concentrações de cianeto de hidrogênio são maiores
que 270 ppm ocorre imediatamente coma e colapso cardiovascular.
Várias tragédias no passado tiveram como pano de fundo o
envenenamento por inalação de vapores de HCN. Grande parte dos plásticos contêm
na sua composição compostos nitrogenados que por combustão libertam gás
cianídrico. Em 1973, em Paris, um incêndio a bordo de um avião matou 119
passageiros e em 1980 em acidente igual morreram 303 peregrinos em Riyadh,
Arábia Saudita, por combustão de material plástico que produziu gás cianídrico.
O cianeto sob a forma de gás é usado para execução nas chamadas câmaras de gás
e foi usado por mais de 900 religiões na Guiana em 1978. O gás cianídrico foi
uma das armas químicas mais recentemente usadas, como por exemplo na guerra do
Golfo (1980-1988) e na agressão iraquiana aos Curdos (1988).
(fonte: www.ff.up.pt/toxicologia/monografias/ano0304/Cianetos/inciah.htm)
Realmente ao que tudo indica, mais uma tragédia que poderia ser
evitada, teve como pano de fundo o HCN.
Amigos, por favor, lutemos por nossos direitos, ou a nosso diversão poderá ser a próxima tragédia nacional
Descansem em paz amigos de Santa Maria.
Amigos, por favor, lutemos por nossos direitos, ou a nosso diversão poderá ser a próxima tragédia nacional
Descansem em paz amigos de Santa Maria.
quarta-feira, 30 de janeiro de 2013
ENEM: exercícios resolvidos sobre modelos atômicos
Olá pessoal! Essa é uma bateria de exercícios sobre modelos atômicos Vamos testar os seus conhecimentos!
1 (Unifor-CE) A descoberta do núcleo atômico está relacionada com experiências realizadas por:
a) Thomson.
b) Milikan.
c) Faraday.
d) Bohr.
e) Rutherford.
2 (UFSM-RS) Considere as afirmativas:
I. O átomo é maciço e indivisível.
II. O átomo é um grande vazio com um núcleo muito pequeno, denso e positivo no centro.
I e II pertencem aos modelos atômicos propostos, respectivamente, por:
a) Dalton e Thomson.
b) Rutherford e Bohr.
c) Dalton e Rutherford.
d) Bohr e Thomson.
e) Thomson e Rutherford.
3 (Unimep-SP) A experiência de Rutherford,
realizada em 1911, consistiu em bombardear lâminas
metálicas com partículas
a) gama.
b) alfa.
c) beta.
d) pósitron.
e) neutrino
4 (UFMG-MG) Na experiência de espalhamento de partículas alfa, conhecida como “experiência de Rutherford”, um feixe de partículas alfa foi dirigido contra uma lâmina finíssima de ouro, e os experimentadores (Geiger e Marsden) observaram que um grande número dessas partículas atravessava a lâmina sem sofrer desvios, mas que um pequeno número sofria desvios muito acentuados. Esse resultado levou Rutherford a modificar o modelo atômico de Thomson, propondo a existência de um núcleo de carga positiva, de tamanho reduzido e com, praticamente, toda a massa do átomo. Assinale a alternativa que apresenta o resultado que era previsto para o experimento de acordo com o modelo de Thomson.
a) A maioria da partículas atravessaria a lâmina
b) A maioria das partículas sofreria grandes desvios ao atravessar a lâmina.
c) A totalidade das partículas atravessaria a lâmina de ouro sem sofrer nenhum desvio.
d) A totalidade das partículas ricochetearia ao se chocar contra a lâmina de ouro, sem conseguir atravessá-la.
5 (PUC-SP) Uma importante contribuição do modelo de Rutherford foi considerar o átomo constituído de:
a) elétrons mergulhados numa massa homogênea de carga positiva.
b) uma estrutura altamente compactada de prótons e elétrons.
c) um núcleo de massa desprezível comparada com a massa do elétron.
d) uma região central com carga negativa chamada núcleo.
e) um núcleo muito pequeno de carga positiva, cercado por elétrons.
6.Assinale a afirmativa a seguir que NÃO é uma idéia que provém do modelo atômico de Dalton.
a) Átomos de um elemento podem ser transformados em átomos de outros elementos por reações químicas.
b) Todos os átomos de um dado elemento têm propriedades idênticas,
as quais diferem das propriedades dos átomos de outros elementos.
c) Um elemento é composto de partículas indivisíveis e diminutas chamadas átomos.
d) Compostos são formados quando átomos de diferentes elementos se combinam em razões bem determinadas.
e) Os átomos são sistemas homogêneos.
7 (UFU-MG) Em 1909, Rutherford e colaboradores reportaram, como resultados de experimentos em que um fluxo de partículas a foi direcionado para uma folha de ouro metálico muito fina, o fato de a grande maioria das
partículas passar pela folha sem mudança de direção e uma pequena quantidade sofrer desvios muito grandes.
Responda:
a) O que é uma partícula ?
b) Por que a maioria das partículas a passaram direto pela folha metálica?
c) Por que uma pequena quantidade de partículas sofreu desvios muito grandes?
8 (Urcamp-RS) Considerando o autor e a ideia, associe a 1ª coluna à 2ª:
a) Dalton ( ) Modelo atômico planetário
b) Rutherford ( ) Átomo indivisível
c) Thomson ( ) Modelo Atômico do ”pudim de passas”
Nesta associação, considerando como associação correta a ordem decrescente, teremos:
a) a, b, c
b) a, c, b
c) c, b, a
d) b, c, a
e) b, a, c
9 (Fuvest-SP) Thomson determinou, pela primeira vez, a relação entre a massa e a carga do elétron, o que pode ser considerado como a descoberta do elétron. É reconhecida como uma contribuição de Thomson ao modelo atômico:
a) o átomo ser indivisível.
b) a existência de partículas subatômicas.
c) os elétrons ocuparem níveis discretos de energia.
d) os elétrons girarem em órbitas circulares ao redor do núcleo.
e) o átomo possuir um núcleo com carga positiva e uma eletrosfera.
10 (ITA-SP) Considerando a experiência de Rutherford, assinale a alternativa falsa:
a) A experiência constitui em bombardear películas metálicas delgadas com partículas alfa.
b) Algumas partículas alfa foram desviadas do seu trajeto devido à repulsão exercida pelo núcleo positivo
do metal.
c) Observando o espectro de difração das partículas alfa, Rutherford concluiu que o átomo tem densidade
uniforme.
d) Essa experiência permitiu descobrir o núcleo atômico e seu tamanho relativo.
e) Rutherford sabia antecipadamente que as partículas alfa eram carregadas positivamente.
11 (UFPA-PA) O modelo probabilístico utilizado para o problema velocidade-posição do elétron é uma consequência do princípio de:
a) Bohr
b) Aufbau
c) De Broglie
d) Heisenberg
e) Pauling
12 (UFMG-MG) De um modo geral, os sucessivos modelos atômicos têm algumas características comuns entre si. Com base na comparação do modelo atual com outros, a afirmativa correta é:
a) no modelo de Dalton e no atual, cada átomo é indivisível.
b) no modelo de Rutherford e no atual, cada átomo tem um núcleo.
c) no modelo de Rutherford e no atual, os elétrons têm energia quantizada.
d) no modelo de Bohr e no atual, os elétrons giram em órbitas circulares ou elípticas.
e) no modelo de Dalton e no atual, as propriedades atômicas dependem do número de prótons.
13 (ITA-SP) Qual das afirmativas a seguir melhor descreve o comportamento de um elétron, comparado com partículas e ondas
tradicionais?
a) É uma partícula que, em certas circunstâncias especiais, se comporta como uma onda.
b) É uma onda que, em certas circunstâncias, se comporta como partícula.
c) À medida que passa o tempo, ora se comporta como partícula, ora como onda.
d) É uma partícula que anda em torno do núcleo, numa trajetória ondulada.
e) Seu comportamento pode ser interpretado como o de partícula ou de onda.
14 (UnB-DF) O entendimento da estrutura dos átomos não é importante apenas para satisfazer à curiosidade dos cientistas: possibilita a produção de novas tecnologias. Um exemplo disso é a descoberta dos raios catódicos, feita pelo físico William Crookes, enquanto estudava as propriedades da eletricidade. Tal descoberta, além de ter contribuído para um melhor entendimento a respeito da constituição da matéria, deu origem aos tubos de imagem de televisores e dos monitores dos computadores. Alguns grandes cientistas que contribuíram para o entendimento da estrutura do átomo foram: Bohr (1885- 1962), Dalton (1766-1844), Rutherford (1871-1937) e Linus Pauling (1901-1994). Com relação à estrutura da matéria, julgue os itens seguintes (Verdadeiro ou Falso):
(0) Ao passar entre duas placas eletricamente carregadas, uma positivamente e outra negativamente, as partículas alfa desviam-se para
o lado da placa negativa.
(1) O átomo é a menor partícula que constitui a matéria.
(2) Cada tipo de elemento químico é caracterizado por um determinado número de massa.
(3) O modelo atômico que representa o comportamento do elétron na forma orbital é o de Rutherford-Bohr.
GABARITO:
1. E
2. C
3. B
4. A
5. C
6. A
7. a) são partículas carregadas, com o núcleo de m.a igual a 4 u.
b) A região onde se encontra o núcleo é 10.000 vezes menor do que o tamanho do átomo, restante é uma espaço vazio.
c) O núcleo é muito mais pesado, sobretudo de Au, do que uma partícula alfa.
8. E
9. C
10. C
11. D
12. B
13. E
14. V F F F
1 (Unifor-CE) A descoberta do núcleo atômico está relacionada com experiências realizadas por:
a) Thomson.
b) Milikan.
c) Faraday.
d) Bohr.
e) Rutherford.
2 (UFSM-RS) Considere as afirmativas:
I. O átomo é maciço e indivisível.
II. O átomo é um grande vazio com um núcleo muito pequeno, denso e positivo no centro.
I e II pertencem aos modelos atômicos propostos, respectivamente, por:
a) Dalton e Thomson.
b) Rutherford e Bohr.
c) Dalton e Rutherford.
d) Bohr e Thomson.
e) Thomson e Rutherford.
3 (Unimep-SP) A experiência de Rutherford,
realizada em 1911, consistiu em bombardear lâminas
metálicas com partículas
a) gama.
b) alfa.
c) beta.
d) pósitron.
e) neutrino
4 (UFMG-MG) Na experiência de espalhamento de partículas alfa, conhecida como “experiência de Rutherford”, um feixe de partículas alfa foi dirigido contra uma lâmina finíssima de ouro, e os experimentadores (Geiger e Marsden) observaram que um grande número dessas partículas atravessava a lâmina sem sofrer desvios, mas que um pequeno número sofria desvios muito acentuados. Esse resultado levou Rutherford a modificar o modelo atômico de Thomson, propondo a existência de um núcleo de carga positiva, de tamanho reduzido e com, praticamente, toda a massa do átomo. Assinale a alternativa que apresenta o resultado que era previsto para o experimento de acordo com o modelo de Thomson.
a) A maioria da partículas atravessaria a lâmina
b) A maioria das partículas sofreria grandes desvios ao atravessar a lâmina.
c) A totalidade das partículas atravessaria a lâmina de ouro sem sofrer nenhum desvio.
d) A totalidade das partículas ricochetearia ao se chocar contra a lâmina de ouro, sem conseguir atravessá-la.
5 (PUC-SP) Uma importante contribuição do modelo de Rutherford foi considerar o átomo constituído de:
a) elétrons mergulhados numa massa homogênea de carga positiva.
b) uma estrutura altamente compactada de prótons e elétrons.
c) um núcleo de massa desprezível comparada com a massa do elétron.
d) uma região central com carga negativa chamada núcleo.
e) um núcleo muito pequeno de carga positiva, cercado por elétrons.
6.Assinale a afirmativa a seguir que NÃO é uma idéia que provém do modelo atômico de Dalton.
a) Átomos de um elemento podem ser transformados em átomos de outros elementos por reações químicas.
b) Todos os átomos de um dado elemento têm propriedades idênticas,
as quais diferem das propriedades dos átomos de outros elementos.
c) Um elemento é composto de partículas indivisíveis e diminutas chamadas átomos.
d) Compostos são formados quando átomos de diferentes elementos se combinam em razões bem determinadas.
e) Os átomos são sistemas homogêneos.
7 (UFU-MG) Em 1909, Rutherford e colaboradores reportaram, como resultados de experimentos em que um fluxo de partículas a foi direcionado para uma folha de ouro metálico muito fina, o fato de a grande maioria das
partículas passar pela folha sem mudança de direção e uma pequena quantidade sofrer desvios muito grandes.
Responda:
a) O que é uma partícula ?
b) Por que a maioria das partículas a passaram direto pela folha metálica?
c) Por que uma pequena quantidade de partículas sofreu desvios muito grandes?
8 (Urcamp-RS) Considerando o autor e a ideia, associe a 1ª coluna à 2ª:
a) Dalton ( ) Modelo atômico planetário
b) Rutherford ( ) Átomo indivisível
c) Thomson ( ) Modelo Atômico do ”pudim de passas”
Nesta associação, considerando como associação correta a ordem decrescente, teremos:
a) a, b, c
b) a, c, b
c) c, b, a
d) b, c, a
e) b, a, c
9 (Fuvest-SP) Thomson determinou, pela primeira vez, a relação entre a massa e a carga do elétron, o que pode ser considerado como a descoberta do elétron. É reconhecida como uma contribuição de Thomson ao modelo atômico:
a) o átomo ser indivisível.
b) a existência de partículas subatômicas.
c) os elétrons ocuparem níveis discretos de energia.
d) os elétrons girarem em órbitas circulares ao redor do núcleo.
e) o átomo possuir um núcleo com carga positiva e uma eletrosfera.
10 (ITA-SP) Considerando a experiência de Rutherford, assinale a alternativa falsa:
a) A experiência constitui em bombardear películas metálicas delgadas com partículas alfa.
b) Algumas partículas alfa foram desviadas do seu trajeto devido à repulsão exercida pelo núcleo positivo
do metal.
c) Observando o espectro de difração das partículas alfa, Rutherford concluiu que o átomo tem densidade
uniforme.
d) Essa experiência permitiu descobrir o núcleo atômico e seu tamanho relativo.
e) Rutherford sabia antecipadamente que as partículas alfa eram carregadas positivamente.
11 (UFPA-PA) O modelo probabilístico utilizado para o problema velocidade-posição do elétron é uma consequência do princípio de:
a) Bohr
b) Aufbau
c) De Broglie
d) Heisenberg
e) Pauling
12 (UFMG-MG) De um modo geral, os sucessivos modelos atômicos têm algumas características comuns entre si. Com base na comparação do modelo atual com outros, a afirmativa correta é:
a) no modelo de Dalton e no atual, cada átomo é indivisível.
b) no modelo de Rutherford e no atual, cada átomo tem um núcleo.
c) no modelo de Rutherford e no atual, os elétrons têm energia quantizada.
d) no modelo de Bohr e no atual, os elétrons giram em órbitas circulares ou elípticas.
e) no modelo de Dalton e no atual, as propriedades atômicas dependem do número de prótons.
13 (ITA-SP) Qual das afirmativas a seguir melhor descreve o comportamento de um elétron, comparado com partículas e ondas
tradicionais?
a) É uma partícula que, em certas circunstâncias especiais, se comporta como uma onda.
b) É uma onda que, em certas circunstâncias, se comporta como partícula.
c) À medida que passa o tempo, ora se comporta como partícula, ora como onda.
d) É uma partícula que anda em torno do núcleo, numa trajetória ondulada.
e) Seu comportamento pode ser interpretado como o de partícula ou de onda.
14 (UnB-DF) O entendimento da estrutura dos átomos não é importante apenas para satisfazer à curiosidade dos cientistas: possibilita a produção de novas tecnologias. Um exemplo disso é a descoberta dos raios catódicos, feita pelo físico William Crookes, enquanto estudava as propriedades da eletricidade. Tal descoberta, além de ter contribuído para um melhor entendimento a respeito da constituição da matéria, deu origem aos tubos de imagem de televisores e dos monitores dos computadores. Alguns grandes cientistas que contribuíram para o entendimento da estrutura do átomo foram: Bohr (1885- 1962), Dalton (1766-1844), Rutherford (1871-1937) e Linus Pauling (1901-1994). Com relação à estrutura da matéria, julgue os itens seguintes (Verdadeiro ou Falso):
(0) Ao passar entre duas placas eletricamente carregadas, uma positivamente e outra negativamente, as partículas alfa desviam-se para
o lado da placa negativa.
(1) O átomo é a menor partícula que constitui a matéria.
(2) Cada tipo de elemento químico é caracterizado por um determinado número de massa.
(3) O modelo atômico que representa o comportamento do elétron na forma orbital é o de Rutherford-Bohr.
GABARITO:
1. E
2. C
3. B
4. A
5. C
6. A
7. a) são partículas carregadas, com o núcleo de m.a igual a 4 u.
b) A região onde se encontra o núcleo é 10.000 vezes menor do que o tamanho do átomo, restante é uma espaço vazio.
c) O núcleo é muito mais pesado, sobretudo de Au, do que uma partícula alfa.
8. E
9. C
10. C
11. D
12. B
13. E
14. V F F F
terça-feira, 22 de janeiro de 2013
ENEM: exercícios sobre separação de misturas e substâncias simples e composta
Pessoal esta é uma bateria sobre química macroscópica. Há exercícios sobre separação de misturas e substâncias simples e composta. Qualquer dúvida sobre o gabarito é só postar aqui.
1) Acerca das mudanças de estado de agregação, considere as afirmações a seguir:
I. Solidificação é a passagem de um material do estado líquido para o estado sólido. O processo ocorre quando
o material é resfriado, caracterizando um fenômeno endotérmico.
II. Considere a mudança de estado: cânfora (sólida) -> cânfora (gasosa)
. Essa mudança de estado é um fenômeno
endotérmico.
III. A mudança do estado gasoso para o estado líquido ocorre com liberação de calor.
Está correto o que afirma em:
a) II e III, apenas.
b) III, apenas.
c) I, II e III.
d) I, apenas.
e) II, apenas.
2) Dentre as inúmeras propriedades curativas atribuídas ao vinagre, este é caracterizado como anti-séptico e antibiótico, sendo então capaz de matar bactérias nocivas à saúde. Quimicamente, o vinagre é constituído pelo ácido acético, que apresenta sob 1 atm de pressão, temperatura de fusão igual a 16,2 o C e temperatura de ebulição entre 116 e 119 oC. Sendo assim, temperaturas em torno de 5 o C favorecem ao vinagre o processo de...
a) fusão.
b) solidificação.
c) condensação.
d) evaporação.
e) sublimação.
3) Marque a alternativa FALSA:
a) A água, o açúcar e o sal (dissolvidos) constituem um sistema monofásico.
b) Uma amostra que apresenta ponto de fusão constante, com certeza corresponde a uma substância pura.
c) Ozônio é uma substância simples do elemento oxigênio.
d) O granito constitui um sistema heterogêneo, pois apresenta três fases.
e) A água mineral filtrada (sem gás) é uma mistura homogênea.
4) Considere uma mistura de três gases A, B e C, que possuem os seguintes pontos de liquefação (PL):
-> Gás A: PL = 0°C
-> Gás B: PL = – 25°C.
-> Gás C: PL = – 40°C.
Pode-se afirmar que:
a) A mistura das três substâncias, a 10°C, será heterogênea.
b) Se a mistura for esfriada a – 30°C, apenas o gás A irá liquefazer.
c) Efetuando-se a liquefação total a mistura e a destilação fracionada, a substância C destilará em primeiro
lugar.
d) Abaixando-se gradativamente a temperatura, o gás C irá liquefazer em primeiro lugar.
e) A mistura, na temperatura de – 60°C, certamente estará no estado gasoso.
5) O vapor obtido pela ebulição das seguintes soluções:
I. Água e sal.
II. Água e açúcar.
III. Água e álcool.
É constituído de água pura apenas:
a) no caso I.
b) no caso II.
c) no caso III.
d) nos casos I e II.
e) nos casos II e III.
6) De uma mistura heterogênea de dois líquidos imiscíveis e de densidades diferentes pode-se obter os líquidos puros por meio de:
I. Sublimação.
II. Decantação.
III. Filtração.
Dessas afirmações, apenas:
a) I é correta.
b) II é correta.
c) III é correta.
d) I e II são corretas.
e) II e III são corretas.
7) (PUC-SP) A flotação é um dos métodos de beneficiamento do carvão mineral. Isso é possível, porque a fração rica em matéria carbonosa e a fração rica em cinzas apresentam diferentes:
a) densidades.
b) pontos de ebulição.
c) estados físicos.
d) pontos de fusão.
e) comportamentos magnéticos.
8) Os fenômenos de EVAPORAÇÃO, CALEFAÇÃO e EBULIÇÃO são formas diferentes de ocorrer uma:
a) fusão
b) solidificação
c) condensação
d) liquefação
e) vaporização
9) Analise as afirmativas abaixo e assinale a alternativa correta:
I. Os compostos Cl2, O2, H2O e C2H4 são todos substâncias simples.
II. Os compostos Cl2, O2, H2O e C2H4 são todos substâncias compostas.
III. É possível separar de uma mistura, de líquidos com pontos de ebulição diferentes, por destilação fracionada.
IV. É possível separar os componentes de uma mistura gasosa por sifonação.
a) I e III são verdadeiras; II e IV são falsas.
b) I, III e IV são verdadeiras; II é falsa.
c) II, III e IV são verdadeiras; I é falsa.
d) I é verdadeira; II, III e IV são falsas.
e) III é verdadeira; I, II e IV são falsas.
10) As propriedades específicas são fundamentais para a identificação das substâncias, pois são características de cada substância. Identifique a alternativa que apresenta apenas propriedades específicas das substâncias.
a) Densidade e solubilidade.
b) Dureza e divisibilidade.
c) Compressibilidade e ductilidade.
d) Ponto de fusão e extensão.
e) Ponto de ebulição e inércia
GABARITO:
1. A
2. B
3. B
4. C
5. D
6. C
7. A
8. E
9. E
10. A
terça-feira, 1 de janeiro de 2013
Sisu 2013: Inscrições do dia 7 a 11 de Janeiro
Seguem as informações do MEC: " Pode fazer a inscrição no Sistema de Seleção Unificada (Sisu) 1º/2013, o estudante que participou do Exame Nacional do Ensino Médio (Enem) de 2012 e obteve nota superior a zero na redação. É necessário informar o número de inscrição e a senha usados no Enem de 2012. Número de inscrição e senha de outras edições do exame não são aceitos."
As inscrições do Sisu estarão disponíveis entre os dias 07 e 11 de janeiro. Para efetuar a inscrição os estudantes deverão informar número de inscrição e senha cadastrados no Enem 2012. Quem tiver esquecido estes dados poderá recuperá-los através do site oficial do Exame.
É possível se inscrever para duas opções de curso. O estudante deverá, no momento da inscrição, especificar sua ordem de preferência e de que forma pretende concorrer – por meio da Lei de Cotas (Lei nº 12.711), de outras políticas afirmativas adotadas pelas instituições participantes do Sisu ou pela ampla concorrência.
A primeira chamada do SISU 2013 será realizada no dia 14 de janeiro e os estudantes selecionados deverão efetuar matrícula diretamente com a instituição nos dias 18, 21 e 22 do mesmo mês. Já a segunda chamada acontece no dia 28 de janeiro e os selecionados deverão entrar em contato com as instituições nos dias 01, 04 e 05 de fevereiro para efetivação da matrícula.
Quem não for selecionado nestas duas primeiras chamadas poderá ainda manifestar o interesse em participar da Lista de Espera do Sisu 2013, no site oficial do sistema, entre os dias 28 de janeiro e 08 de fevereiro. A partir do dia 18 de fevereiro as próprias instituições farão uso desta lista para convocar os candidatos para ocuparem as vagas eventualmente não ocupadas.
O período de inscrição é bem curto, então fiquem atentos!! Sabemos o número do acessos será enorme, então não deixe para a última hora!!
Boa Sorte!!
Assinar:
Postagens (Atom)



